版权所有 辽宁海泰科技发展有限公司
市场营销地址:辽宁省抚顺市望花区裕宝新城1号楼1单元31层
生产厂地址:中国辽宁省沈抚新区青台子路38号
邮编:113122 邮箱:sales@chinacatalyst.com
辽ICP备2022002379号-1 网站建设:中企动力沈阳 手机版 邮箱
从FDS-4A型加氢精制催化剂中回收分离钴、钼
分类:
知识窗
作者:
来源:
发布时间:
2010-12-31
杨万军,杨晓美,王伟
(吉林市吉清科技开发有限公司,吉林132021)
0 前言
钴、钼两种元素均是稀有金属。在地壳中含量仅有0.001% ~0.005% 。然而两种金属的用途却十分广泛。就钴而言,工业上有75% ~80% 的钴用于制造超热合金、永久磁铁、硬质、精密、抗腐、焊接和低膨胀系数等各种含钴合金。有15% ~20% 的钴用于搪瓷、陶瓷颜料制造业中;有5% ~10% 的钴用于工业催化剂中。钼在工业中的用途更为广泛,主要用于特种钢材的生产,在钢材中加入少量的金属钼,就可以改变钢材原有的品质,提高了钢材的硬度、轫性、抗腐蚀、抗高温、抗蠕变能力。同时,钼在航天、电子、原子能、轻工、化工工业上也有广泛的应用。随着我国及世界石油化工工业的发展,钴、钼作为石油炼制催化剂中的重要活性组分,在石油化工工业上应用日趋得到发展。而每年从石油化工工业装置上卸下来的含钴、钼金属废催化剂近千吨。因此,我们将其做为二次资源回收利用具有非常重要的意义。
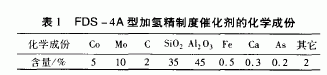
1 FDS-4A型加氢精制废催化剂的化学成分构成
2 从FDS-4A型废催化剂中提取钴、钼工艺
针对废催化剂的成分构成,我们首先将废催化剂于550℃进行焙烧,使废催化剂表面吸附的碳、硫、碳氢化合物等氧化成二氧化碳、二氧化硫被除去。同时也使催化剂中毒时吸附的重金属砷挥发掉,在此过程中,钴、钼均变成金属氧化物。然后用氢氧化钠溶液控制一定的pH值将钼浸取,浸渣水洗后,用盐酸浸取,使渣中的钴生成氯化钴进人浸液中。分别将得到的钼酸钠、氯化钴浸液净化。钼酸钠净化液采用蒸发结晶工艺使其呈结晶状态从净化液中析出;在氯化钴净化液中加入适量的草酸铵,使钴以草酸钴的形式从溶液中析出,再经烘干、锻烧得氧化钴。
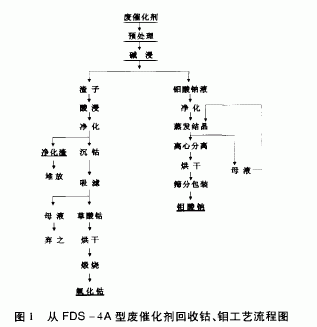
3 工艺流程图
4 工序过程中钴、钼及其它成分的行为分析及条件
4.1 原料预处理过程的成分行为分析
FDS一4A型加氢精制催化剂在制备过程中,采用的是混捏碾磨法。活性组分钴、钼与载体均匀混合后,经压片成型。在催化剂使用过程中活性组分的表面,吸附着大量的硫、碳、碳氢化合物及重金属砷等,使催化剂失去了活性。如果直接用碱或酸对催化剂进行浸出提取,很难得到满意的效果,即使能够从载体上将活性组分浸取下来。又由于有大量的碳在浸液中,对有价活性组分有强烈的吸附作用,使活性组分的实际收率大大降低。对此我们将废催化剂先进行焙烧,将有机物、硫、重金属砷等氧化挥发掉,同时使有价金属钴氧化成CoO或Co2O3,钼氧化成易于浸取的MoO3,其它金属杂质也变成相应的氧化物。废催化剂焙烧的过程,也就是催化剂中的活性组分得到活化的过程。在此过程中,钴、钼将损失0.5% 。
2Co + O2=2CoO
4CoO +O2↑= 2Co2O3
2Mo+301=2MoO3
C+O2=CO2↑
S+O = SO2↑
2As + O3=As2O3
4Fe + 302=2Fe2O3
4.2 碱浸过程中各成分行为分析
将焙烧后的废催化剂粉碎,过40目筛网。按1:3~4的固液比在搅拌下加到氢氧化钠的溶液中,于95~100℃恒温浸取1.5~2.0 h,并用氢氧化钠调浸液pH 值为8~8.5,抑制硅及钴浸到溶液中。在浸取过程中,催化剂中的MoO 、CaO和少量的si、Al等其它可溶性杂质进到浸液中,而CoO、Co O 和大部分的SiO 、AI:O 、Fe:O,等留在浸渣中,使钼与钴在此过程中得以分离。物料粉碎的目的就是增加物料与浸液的接触面积,提高浸取效果。在碱浸过程中,钼的浸出率为96% 。
MoO3+2NaOH = Na2MoO4+H2O
CaO+H2O =Ca(OH)2
SiO2+2NaOH=2NaSiO3+H2O
4.3 钼酸钠液净化过程中杂质的行为
钼酸钠浸液热滤后,溶液中仍含有少量未沉淀完全的可聚集沉降的絮状物。可将溶液自然冷却,静置16 h以上,使杂质聚集沉淀完全。过滤后,再用氢氧化钠调溶液pH=10~l0.5。加热浓缩,至溶液密度d=1.35 g/cm3,此时有少量悬浮物在溶液中,溶液呈混浊状,冷却后过滤,使其除去。滤液经蒸发、结晶、烘干、筛分、包装即得合格的钼酸钠产品。
4.4 碱浸渣酸浸过程中各成分行为分析
废催化剂碱浸后的渣子中主要成分为:CoO、Co2O3、SiO2、A12O3、Fe2O3、CaO等。将吸干后的湿渣按1:3的固液比在搅拌下加到3N的盐酸中,于80~85 恒温浸取1.5~2.0 h。
为了加快化学反应,缩短反应时间,提高浸取质量,在浸取过程中可加人物料量10% ~15% 的硝酸。在浸取过程中,物料中的CoO、Co2O3,、Fe2O3、CaO等与酸反应,分别生成相应的化合物,CoC12、Co(NO3)2,、FeC13、CaCI2,等。
CoO 十2HC1=CoC12+H2O
Co2O3+6HC1=2COC12+3H2O +Cl2
Fe2O3+6HC1=2FeC13+3H2O
CaO 十2HCI=CaCI2+H2O
4.5 氯化钴浸取液净化过程中各组分的行为分析
在“4.4”所得到的氯化钴浸取液中,主要含有CoC12、FeC13 和少量CaC1 及其它微量杂质,该溶液的净化主要是将溶液中的e3+ 和少量Ca“等去除。首先,用1:3的稀氨水,在搅拌下于50℃慢慢将溶液pH值调至4.0~4.2,在此过程中,应不断仔细观察和用试纸进行检查,当pH:4.0~4.2时,将浆液加热沸腾15~20min,使生成的Fe(OH) 凝聚成大颗粒而沉淀:待净化液中Fe3+检测合格后,放料过滤,滤渣水洗后堆放,滤液去草酸钴沉淀工序。在此过程中所得到的CoCI,净化液必须清彻透明,溶液中的铁含量必须达到技术要求。
Fe3++3OH-=Fe(OH)3↓
4.6 草酸钴沉淀过程中条件的控制
净化后的CoCI,溶液中,主要含有CoCI 及少量杂质ca2+、Fe3+ 、Na+ 等。当向溶液中加入草酸铵时,溶液中的钴以草酸钴的形式从溶液中沉淀析出。为了使草酸钴沉淀过程中尽量少夹带杂质,我们采取了如下措施:
(1)控制CoCI2溶液的浓度在50g/L·Co,草酸铵密度1.03 g/cm ;
(2)沉淀前将CoCI 溶液用草酸酸化抑制Ca的沉淀;
(3)控制草酸钴沉淀过程中溶液的温度在36~42℃ :
(4)控制草酸铵的加入量,使母液中预留一部分钴2~3 g/L
(5)沉淀结束后,立即过滤,防止杂质产生后沉淀现象,影响产品质量;
(6)用70~80℃热水洗草酸钴2~3次;
(7)草酸铵的加入方式采用细流分散喷入:
CoCI2H2C2O4=CoC2O4+2H
Fe3+ +3C2O4-=[Fe(C2O3)3]
通过采取上述措施,可得到理想的草酸钴产品,母液进行二次沉钴,在该过程钴回收率为99% 。
4.7 草酸钴的干燥、煅烧
4.7.1 基本原理
干燥的目的是除去沉淀物外表吸附的游离水份,然后在400~450 cc下煅烧成黑色产物。
2CoC2O4+O2↑=2CoO +CO2↑
4CoC2O4+O2↑2Co!O3+4CO2↑+4C0↑
3CoC2O4+O2↑=Co3O4+4CO2↑ +2CO↑
4.7.2 草酸钴煅烧的工艺条件分析
(1)煅烧温度:400~450℃。分解温度低,生成的氧化钴粉末细,且产品外观模糊。温度高,颗粒长大快,易产生烧结。
(2)煅烧时间:5~6 h。具体因料层薄厚、翻动次数、原料的干湿而定。
(3)产品粒度:烧后产品过40目筛网。
5 钼酸钠、氧化钴产品质量标准及回收产品分析数据
5.1 钼酸钠产品质量标准及回收产品分析数据
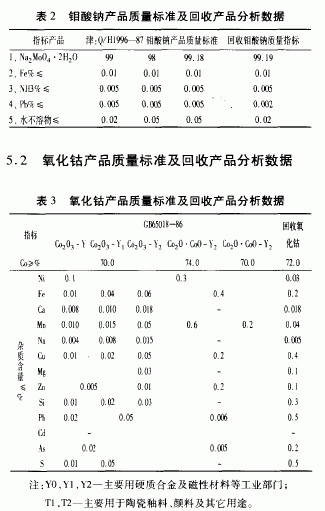
6 经济技术指标
6.1 各工序中钼、钴收率
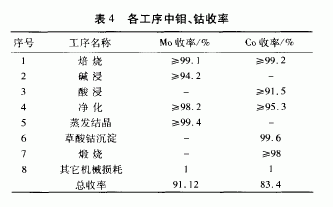
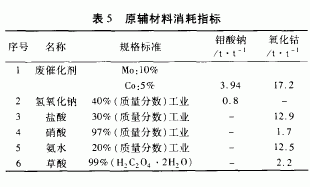
6.2 原辅材料消耗指标
7 结 论
以FDS一4A型加氢精制废催化剂为原料,采用焙烧、碱浸、酸浸、净化、蒸发结晶、草酸铵沉钴及煅烧工艺路线,生产出的钼酸钠、氧化钴产品,其产品质量符合国家标准,说明该工艺是可行的。对于从废催化剂中回收有价金属工艺路线,不能干篇一律,一成不变,既要考虑到催化剂载体构成,催化剂的制备方法,催化剂在使用过程中成分的变化,同时也要考虑活性组分的构成,活性组分存在状态,杂质的构成等相关因素。综合上述种种因素后,方能确定出一条合理的工艺路线,达到分离,提纯金属元素的目的。杨万军,杨晓美,王伟
(吉林市吉清科技开发有限公司,吉林132021)
0 前言
钴、钼两种元素均是稀有金属。在地壳中含量仅有0.001% ~0.005% 。然而两种金属的用途却十分广泛。就钴而言,工业上有75% ~80% 的钴用于制造超热合金、永久磁铁、硬质、精密、抗腐、焊接和低膨胀系数等各种含钴合金。有15% ~20% 的钴用于搪瓷、陶瓷颜料制造业中;有5% ~10% 的钴用于工业催化剂中。钼在工业中的用途更为广泛,主要用于特种钢材的生产,在钢材中加入少量的金属钼,就可以改变钢材原有的品质,提高了钢材的硬度、轫性、抗腐蚀、抗高温、抗蠕变能力。同时,钼在航天、电子、原子能、轻工、化工工业上也有广泛的应用。随着我国及世界石油化工工业的发展,钴、钼作为石油炼制催化剂中的重要活性组分,在石油化工工业上应用日趋得到发展。而每年从石油化工工业装置上卸下来的含钴、钼金属废催化剂近千吨。因此,我们将其做为二次资源回收利用具有非常重要的意义。
1 FDS-4A型加氢精制废催化剂的化学成分构成
2 从FDS-4A型废催化剂中提取钴、钼工艺
针对废催化剂的成分构成,我们首先将废催化剂于550℃进行焙烧,使废催化剂表面吸附的碳、硫、碳氢化合物等氧化成二氧化碳、二氧化硫被除去。同时也使催化剂中毒时吸附的重金属砷挥发掉,在此过程中,钴、钼均变成金属氧化物。然后用氢氧化钠溶液控制一定的pH值将钼浸取,浸渣水洗后,用盐酸浸取,使渣中的钴生成氯化钴进人浸液中。分别将得到的钼酸钠、氯化钴浸液净化。钼酸钠净化液采用蒸发结晶工艺使其呈结晶状态从净化液中析出;在氯化钴净化液中加入适量的草酸铵,使钴以草酸钴的形式从溶液中析出,再经烘干、锻烧得氧化钴。
3 工艺流程图
4 工序过程中钴、钼及其它成分的行为分析及条件
4.1 原料预处理过程的成分行为分析
FDS一4A型加氢精制催化剂在制备过程中,采用的是混捏碾磨法。活性组分钴、钼与载体均匀混合后,经压片成型。在催化剂使用过程中活性组分的表面,吸附着大量的硫、碳、碳氢化合物及重金属砷等,使催化剂失去了活性。如果直接用碱或酸对催化剂进行浸出提取,很难得到满意的效果,即使能够从载体上将活性组分浸取下来。又由于有大量的碳在浸液中,对有价活性组分有强烈的吸附作用,使活性组分的实际收率大大降低。对此我们将废催化剂先进行焙烧,将有机物、硫、重金属砷等氧化挥发掉,同时使有价金属钴氧化成CoO或Co2O3,钼氧化成易于浸取的MoO3,其它金属杂质也变成相应的氧化物。废催化剂焙烧的过程,也就是催化剂中的活性组分得到活化的过程。在此过程中,钴、钼将损失0.5% 。
2Co + O2=2CoO
4CoO +O2↑= 2Co2O3
2Mo+301=2MoO3
C+O2=CO2↑
S+O = SO2↑
2As + O3=As2O3
4Fe + 302=2Fe2O3
4.2 碱浸过程中各成分行为分析
将焙烧后的废催化剂粉碎,过40目筛网。按1:3~4的固液比在搅拌下加到氢氧化钠的溶液中,于95~100℃恒温浸取1.5~2.0 h,并用氢氧化钠调浸液pH 值为8~8.5,抑制硅及钴浸到溶液中。在浸取过程中,催化剂中的MoO 、CaO和少量的si、Al等其它可溶性杂质进到浸液中,而CoO、Co O 和大部分的SiO 、AI:O 、Fe:O,等留在浸渣中,使钼与钴在此过程中得以分离。物料粉碎的目的就是增加物料与浸液的接触面积,提高浸取效果。在碱浸过程中,钼的浸出率为96% 。
MoO3+2NaOH = Na2MoO4+H2O
CaO+H2O =Ca(OH)2
SiO2+2NaOH=2NaSiO3+H2O
4.3 钼酸钠液净化过程中杂质的行为
钼酸钠浸液热滤后,溶液中仍含有少量未沉淀完全的可聚集沉降的絮状物。可将溶液自然冷却,静置16 h以上,使杂质聚集沉淀完全。过滤后,再用氢氧化钠调溶液pH=10~l0.5。加热浓缩,至溶液密度d=1.35 g/cm3,此时有少量悬浮物在溶液中,溶液呈混浊状,冷却后过滤,使其除去。滤液经蒸发、结晶、烘干、筛分、包装即得合格的钼酸钠产品。
4.4 碱浸渣酸浸过程中各成分行为分析
废催化剂碱浸后的渣子中主要成分为:CoO、Co2O3、SiO2、A12O3、Fe2O3、CaO等。将吸干后的湿渣按1:3的固液比在搅拌下加到3N的盐酸中,于80~85 恒温浸取1.5~2.0 h。
为了加快化学反应,缩短反应时间,提高浸取质量,在浸取过程中可加人物料量10% ~15% 的硝酸。在浸取过程中,物料中的CoO、Co2O3,、Fe2O3、CaO等与酸反应,分别生成相应的化合物,CoC12、Co(NO3)2,、FeC13、CaCI2,等。
CoO 十2HC1=CoC12+H2O
Co2O3+6HC1=2COC12+3H2O +Cl2
Fe2O3+6HC1=2FeC13+3H2O
CaO 十2HCI=CaCI2+H2O
4.5 氯化钴浸取液净化过程中各组分的行为分析
在“4.4”所得到的氯化钴浸取液中,主要含有CoC12、FeC13 和少量CaC1 及其它微量杂质,该溶液的净化主要是将溶液中的e3+ 和少量Ca“等去除。首先,用1:3的稀氨水,在搅拌下于50℃慢慢将溶液pH值调至4.0~4.2,在此过程中,应不断仔细观察和用试纸进行检查,当pH:4.0~4.2时,将浆液加热沸腾15~20min,使生成的Fe(OH) 凝聚成大颗粒而沉淀:待净化液中Fe3+检测合格后,放料过滤,滤渣水洗后堆放,滤液去草酸钴沉淀工序。在此过程中所得到的CoCI,净化液必须清彻透明,溶液中的铁含量必须达到技术要求。
Fe3++3OH-=Fe(OH)3↓
4.6 草酸钴沉淀过程中条件的控制
净化后的CoCI,溶液中,主要含有CoCI 及少量杂质ca2+、Fe3+ 、Na+ 等。当向溶液中加入草酸铵时,溶液中的钴以草酸钴的形式从溶液中沉淀析出。为了使草酸钴沉淀过程中尽量少夹带杂质,我们采取了如下措施:
(1)控制CoCI2溶液的浓度在50g/L·Co,草酸铵密度1.03 g/cm ;
(2)沉淀前将CoCI 溶液用草酸酸化抑制Ca的沉淀;
(3)控制草酸钴沉淀过程中溶液的温度在36~42℃ :
(4)控制草酸铵的加入量,使母液中预留一部分钴2~3 g/L
(5)沉淀结束后,立即过滤,防止杂质产生后沉淀现象,影响产品质量;
(6)用70~80℃热水洗草酸钴2~3次;
(7)草酸铵的加入方式采用细流分散喷入:
CoCI2H2C2O4=CoC2O4+2H
Fe3+ +3C2O4-=[Fe(C2O3)3]
通过采取上述措施,可得到理想的草酸钴产品,母液进行二次沉钴,在该过程钴回收率为99% 。
4.7 草酸钴的干燥、煅烧
4.7.1 基本原理
干燥的目的是除去沉淀物外表吸附的游离水份,然后在400~450 cc下煅烧成黑色产物。
2CoC2O4+O2↑=2CoO +CO2↑
4CoC2O4+O2↑2Co!O3+4CO2↑+4C0↑
3CoC2O4+O2↑=Co3O4+4CO2↑ +2CO↑
4.7.2 草酸钴煅烧的工艺条件分析
(1)煅烧温度:400~450℃。分解温度低,生成的氧化钴粉末细,且产品外观模糊。温度高,颗粒长大快,易产生烧结。
(2)煅烧时间:5~6 h。具体因料层薄厚、翻动次数、原料的干湿而定。
(3)产品粒度:烧后产品过40目筛网。
5 钼酸钠、氧化钴产品质量标准及回收产品分析数据
5.1 钼酸钠产品质量标准及回收产品分析数据
6 经济技术指标
6.1 各工序中钼、钴收率
6.2 原辅材料消耗指标
7 结 论
以FDS一4A型加氢精制废催化剂为原料,采用焙烧、碱浸、酸浸、净化、蒸发结晶、草酸铵沉钴及煅烧工艺路线,生产出的钼酸钠、氧化钴产品,其产品质量符合国家标准,说明该工艺是可行的。对于从废催化剂中回收有价金属工艺路线,不能干篇一律,一成不变,既要考虑到催化剂载体构成,催化剂的制备方法,催化剂在使用过程中成分的变化,同时也要考虑活性组分的构成,活性组分存在状态,杂质的构成等相关因素。综合上述种种因素后,方能确定出一条合理的工艺路线,达到分离,提纯金属元素的目的。
上一篇:
汽车尾气净化三效催化剂的研究进展






